La Food and Drug Administration (FDA) de los EE. UU., la Comisión Europea y otros organismos reguladores han convertido la seguridad de los pacientes en una prioridad estratégica mediante el desarrollo de una legislación relativa a un sistema de identificación única del producto (sistema UDI).
El 26 de Mayo de 2021, es la nueva fecha de entrada en vigor del nuevo reglamento europeo, a causa del COVID-19.
Para ayudarte a cumplir con el reglamento, desde AECOC ponemos a tu disposición diferentes herramientas y servicios que permitirán a tu compañía adaptarse a los nuevos requerimientos.
¿Quieres más información?
Ponte en contacto con: estandaresgs1@aecoc.esDocumentación relacionada
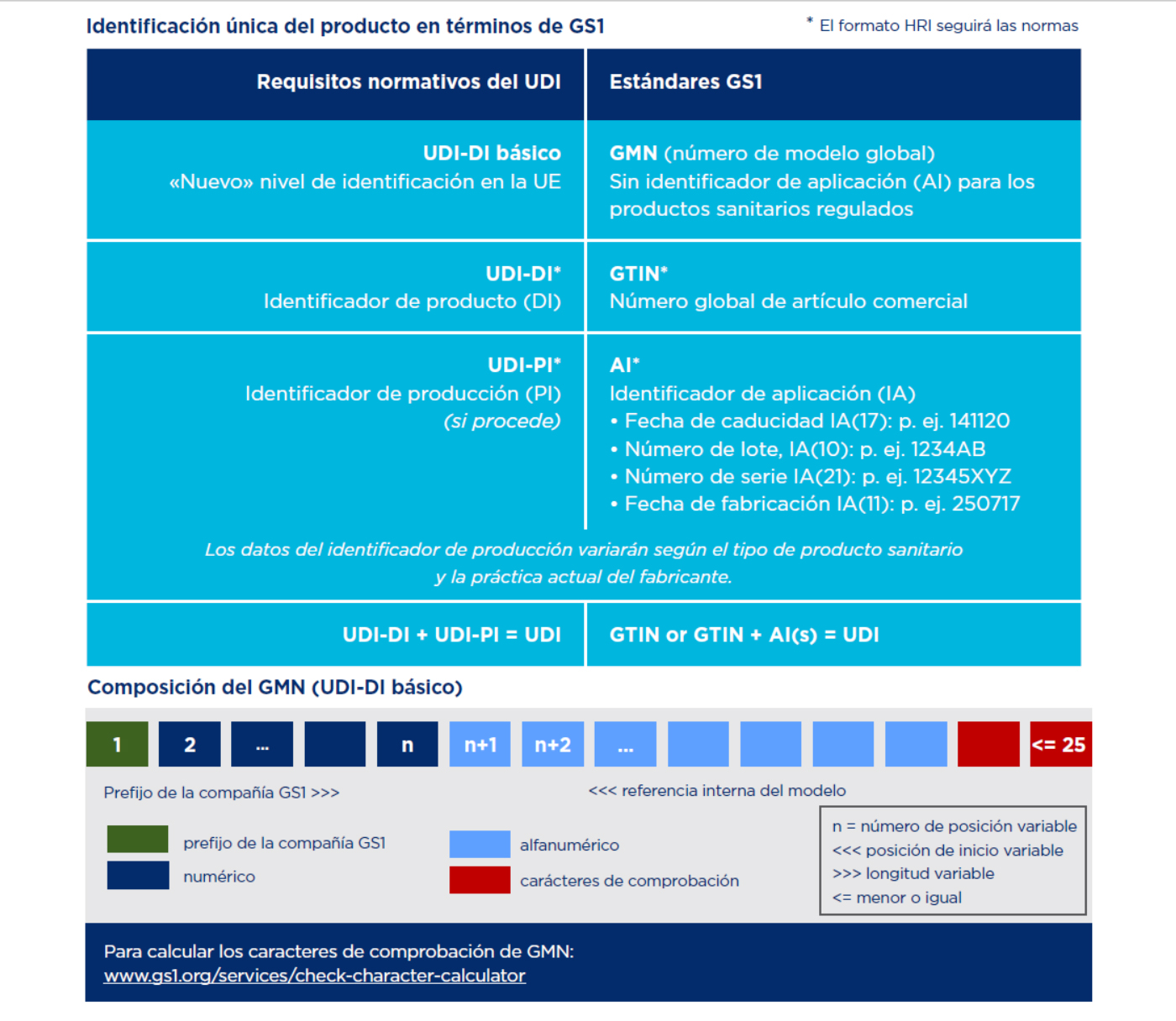
Esta guía recoge la información básica para prepararse para la implementación del sistema de identificación única para los productos sanitarios (UDI)
La presente Guía de codificación ofrece a todos los agentes del sector sanitario, una aproximación clara y sencilla a los estándares GS1
Guía con información básica sobre el sistema de identificación única de producto (UDI) así como de la composición del GMN (UDI-DI básico) y del GTIN (UDI-DI).
El Diario Oficial de la Unión Europea publica el Reglamento (UE) 2020/561 por el que se modifica el Reglamento (EU) 2017/745 aplazando un año la fecha de aplicación del Reglamento sobre los productos sanitarios, pasando a ser en vez de 26 de mayo de 2020, el 26 de mayo de 2021.
Formación relacionada
Identificación única de Productos Sanitario (UDI): US, UK y EU
CURSO
Conozca las bases para implantar correctamente Códigos de Barras, EDI y AECOC DATA

Primeros pasos para poner en marcha los Estándares GS1 Salud: Serialización, UDI, EDI y AECOC DATA
WEBINAR
Conozca las bases para implantar correctamente Códigos de Barras, EDI y AECOC DATA